目前華人疾病大宗為肝病(癌)、糖尿病併發症等,集團旗下合一(4743-TW)的抗糖尿病足新藥ON101,有機會獲得美國食品藥物管理局(FDA)突破性療法資格,抗C肝、肝癌藥也將積極聚焦大陸市場。
2015-05-06 經濟日報 記者黃文奇/台北報導
近年來以天然草本植物來源為基礎的藥物開發,逐漸引起製藥產業的注意,隨著老年人口漸增及消費者追求天然的趨勢,市場需求一直有增無減,植物藥已廣泛地運用於疾病治療及疾病症狀的改善。且因目前部份小分子化學藥物毒性高、副作用較大,許多重大疾病 ,如癌症、老年癡呆症、神經系統疾病、免疫治療、類風濕性關節炎等的治療效果仍有很大的改善空間,更加提升了大眾對於植物新藥開發的期待。
台灣具有中國數千年文化傳承的底子,在植物藥方面的使用已有豐富的經驗,廠商目前也極力推廣植物藥的國際地位,開發中的植物新藥案件也逐漸增加,以未被滿足的醫療需求為主要目標市場,若能成功踏上國際舞台,則能帶動整個台灣的產業發展。
產業知識
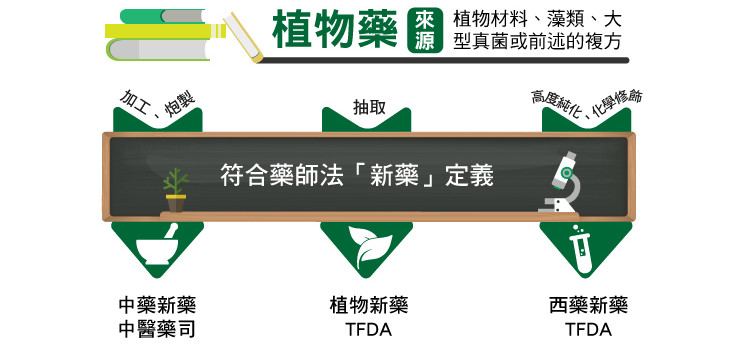
以植物為來源的藥品根據製程及萃取純化的程度不同,而可經不同的法源、不同的身分申請上市。
中藥新藥
以中醫理論為基礎,使用防治疾病功能植物、動物、礦物以及其加工品,為人類治療或預防疾病之藥材,不論產地,稱為中藥。為了提升醫療品質與用藥安全,即使是已有數千年傳統的中醫/中藥系統,也順應時勢,建立中藥相關管理法規,走向更明確、更有科學依據,不只強調療效更著重安全性。
列於傳統方劑典籍之中藥欲用於新的疾病或使用途徑;沒有傳統使用經驗卻在國外被廣泛使用,且列於該國家藥典之植物藥;新使用之藥用部位;新複方。以上這些都可以依循中藥新藥管理法規申請上市,若有需要,亦須進行臨床試驗,且台灣目前已設立多個中藥臨床試驗中心,期望提供給民眾更安全有效的中醫藥環境。
植物藥新藥
無論是以植物材料、藻類、大型真菌或前述的複方為來源之抽取物所製成的藥品,且符合中央衛生主管機關審查認定屬新成分、新療效複方或新使用途徑製劑之藥品,即可稱為植物新藥。
不似西藥,只以單一成分為有效成分,申請上市時也不一定要對活性成分進行定性,卻也不像中藥方劑,已完整在傳統方劑典籍中記載詳細使用資料,整體而言,植物藥新藥介於中藥與西藥之間,包含了兩者的特性,管理機關則與西藥同為食品藥物管理署(TFDA)。
西藥新藥
若經基因轉殖、以植物為來源但已經過高度純化的物質(以其中單一成份做成藥品,如抗癌藥紫杉醇)、或是經化學修飾(加入人工化學改良,如山藥萃取合成的雌激素),則僅有其植物性部分屬於此規範內,例如如若該藥品含有大豆萃取物及以山藥萃取物合成的雌激素,「植物藥新藥查驗登記基準」只適用於大豆萃取物的部分。
合一在產業中的商機
合一為新藥研發型生技公司,經營形態不同於一般生產製造為主的公司,銷售策略亦有別於一般製造型公司,主要銷售政策如下:
(1) 階段性產品技術授權。
(2) 深耕國內外行銷通路與客戶服務。
(3) 針對客戶需求研發新系列產品,以滿足市場需求。
(4) 積極參加國內外之生物科技展覽活動,以利市場行銷拓展。
保健品目前以透過李時珍本草屋行銷系統銷售為主,同時也進一步積極與各大藥局通路簽訂區域經銷合約,於各中醫藥、西藥局與藥妝等通路經銷本公司產品。另外亦進行網路行銷與網購佈局,以增進產品銷售的便利性與營業額。由於國內屬於淺碟性市場,市場規模有限且易於飽和,積極擴充台灣以外的市場十分重要,因此,利用在中國市場已佈建之通路銷售公司之產品,並尋求技術或產品的授權機會,進而拓展東南亞及亞洲市場,為公司未來主要銷售政策之一環。
基於新藥研發時程長的特性,短期內要有新藥產品上市不易,因而在新藥銷售政策上採取以階段性價值進行技術授權的模式為主,也就是新藥產品完成階段性研發,賦與產品附加價值後進行授權,授權對象涵蓋國內外之廠商,授權模式則包括全球獨家授權、部分區域國家獨家授權等,公司亦不排除藉由合作開發及策略聯盟方式與國際藥廠共同開發至產品成功上市,以累積寶貴新藥開發經驗,並藉以收取授權金及產品上市後之權利金,期於較短時間內產生收益,增加公司之價值。
目前之商品(服務)項目
(A) 新藥開發主要計劃項目:
- ON101:主要療效為慢性糖尿病足部潰瘍傷口癒合新藥。
- OB318:主要療效為抗癌。
(B) 保健產品:
- 保健用品:合一本草抗荳修護霜、寶貝護臀霜、刮鬍膏;喜樂療却痘修護霜;到手香萬用軟膏、敏康軟膏、到手香膏、荳康、寶康、牙膏、漱口水等。
- 保健食品:葡萄糖胺液。
- 健康食品:牛樟芝菌絲體。
市場概況
近年來,全球植物藥市場蓬勃發展,估計每年平均以10~20%的速度快速成長,至2011年,全球植物藥市場達260億美元的規模。而依據BCC公司的調查顯示,全球植物新藥(Botanical Drug)及植物衍生藥品(Plant-Derived Drugs)的市場,亦將由2008年的195億美元大幅成長至2013年的329億美元,平均年複合成長率達11% 。其中,歐、美為全球使用植物藥最多、應用最廣的地區,北美的植物藥市場已占全球植物藥市場的50%以上,且市場成長的速度超過西歐及亞洲市場,至2011年北美的植物藥市場占全球的54%,在美國、加拿大及歐洲售出的處方藥中,約有1/4的有效成分是來自於植物。
目前25萬種植物中,僅約5-15%有效成分被發現,尚有極多活性成分待發掘,因此藥廠及科學家致力於從植物中找尋具有生物活性的新成分,並開發為新藥。截至目前為止,美國已有兩項植物新藥被核准上市,植物藥取得新藥上市許可的標準逐漸建立並明朗,在此前提下,BCC推估,隨著未來植物新藥核准上市數量越來越多,市場將大幅成長。
植物新藥近年來逐漸在歐美各國流行,全球現已有45%的人口使用植物藥養生或治病。植物藥的風潮席捲全球,其中又以中國、日本、韓國、德國及美國,分別是亞洲、歐洲及美洲三個地區發展植物藥的代表。因應植物藥的快速發展,由歐盟各國到美國,再到亞洲各國,紛紛成立植物藥的管理單位,其中德國最具規模,並同時建立保險制度。美國(FDA)更是制訂了管理植物藥的標準,並於2004年6月公告「植物藥品審查準則」。我國除制訂中草藥五年發展計畫,投入約五十億元,由生技中心、生醫中心與藥技中心建立植物藥研發與產品技術平台,協助民間研發植物藥,並由衛生單位建立管理法規,繼2009年3月31日藥政處(現TFDA)公告植物藥新藥臨床試驗基準後,更領先全球於2013年4月17日公告「植物藥新藥查驗登記審查基準」,使植物藥研究開發工作及查驗登記能有明確的法規可供遵循。
產業上中下游
製藥產業之上游,係製備藥物加工的原材料階段。原材料分別有來自化學品、天然植物、動物、礦物、微生物菌種及相關的動植物細胞等,其中以一般化學為原材料占大多數,植物藥的上游藥材,則主要以植物作為原料。近幾年來由於生物技術的進展,利用基因工程製造的基因轉殖動物與植物,也可以直接做為生產藥材。
製藥產業之中游,主要為原料藥工業及植物藥材加工階段。原料藥工業基本上為有機化學工業,原料的製備有從天然物取得者,有從微生物發酵或動植物細胞培養而來,主要製程技術在回收、萃取、分離、純化及製劑配方;由一般化學品製備者,主要製程技術為複雜的有機合成及分離純化,由微生物、動物、植物細胞製備者無論是抗生素、蛋白質藥物、單株抗體等,則亦有回收、純化、製劑配方等加工。
植物藥材的加工則以藥用植物加工、炮製及加上賦形劑、崩散劑、粘著劑、潤滑劑等製備為方便使用的劑型。植物藥裡面的中藥除了可依傳統方法將藥材加工成膏、散、丹、丸等傳統劑型外,目前已有許多的工廠將中藥方劑,提煉濃縮加工生產成西藥劑型,稱之為科學中藥。
製藥產業之下游,係指傳統中藥、科學中藥、處方藥及成藥之行銷通路商,如中藥房、中醫院、各醫療診所、藥局、健保局及藥妝店等,透過醫師開立處方箋後由藥劑師調劑,或由醫師、藥師自行處方,送交終端消費者。
長、短期業務發展計畫
- 長期業務發展計畫
(1) ON101 繼完成第二期臨床後,規劃並執行第三期大型人體臨床試驗,並藉由技術授權、合作開發、及策略聯盟方式與國際藥廠共同開發,累積寶貴新藥開發經驗至產品成功上市,同時公司可由合作協議中收取高額之授權費,及產品上市後之權利金。此外,ON101 一旦成功開發成為糖尿病足部慢性潰瘍新藥,ON101 對其它傷口的適應症亦將陸續成為未來長期的研發標的。
(2) 合一生技將發展牛樟芝抗癌新藥視為公司長遠計畫之一。由於此新藥為分離純化自牛樟芝之純化合物,未來需依小分子新藥的法規要求進行研發,雖時程較為漫長,但其抗肝癌及乳癌市場極為龐大,具有無窮之開發潛力。
(3) 於國際主要地區規劃並保有新藥之開發、製造、銷售權以獲得最大利潤。未來引進新藥開發計畫著重於評估已完成初期開發,具有市場性及成功率較高的新藥技術或專利授權。 - 短期業務發展計畫
(1) 本公司未來短、中期計畫主要為完成糖尿病傷口癒合新藥ON101 的期中分析,以初步確立大規模使用下的療效及安全性,增加ON101 的階段性價值,吸引國際大廠的投資。此外,基於市場性及全球缺乏糖尿病慢性足部潰瘍藥,公司於短、中期計畫中規劃開啟ON101 多國多中心臨床試驗,將陸續向美、中、香港等國家提出三期臨床試驗的許可。
(2) 合一生技將發展牛樟芝抗癌新藥進入臨床試驗視為公司短期計畫之一。不論OB318 亦為植物提取、部分純化的極單純植物萃取物,經細胞及動物試驗證實生體內外的療效與明確作用機制,目前已完成CMC 研究並積極執行藥/毒理及藥動學等多方面的臨床前測試,該項產品估計將於短時間內完成臨床前試驗後進入人體臨床,使公司新藥研發得永續經營,亦為公司短期的重大目標。
(3) 利用本公司專屬擁有的特定植物萃取技術平台,開發一系列具有科學驗證基礎之皮膚修復、滋潤及保養的產品或非處方用藥,以創造階段性的附加價值。
(4) 本公司已建立符合GAP 標準的到手香大規模生產基地,量產成功後可提供充足且品質穏定的到手香藥材,不僅確保ON101 第三期臨床試驗用藥的供應與未來生產所需,更能用以生產全方位的系列保健、保養用品,挹注新藥開發成功前的短期營收。
大事件紀錄
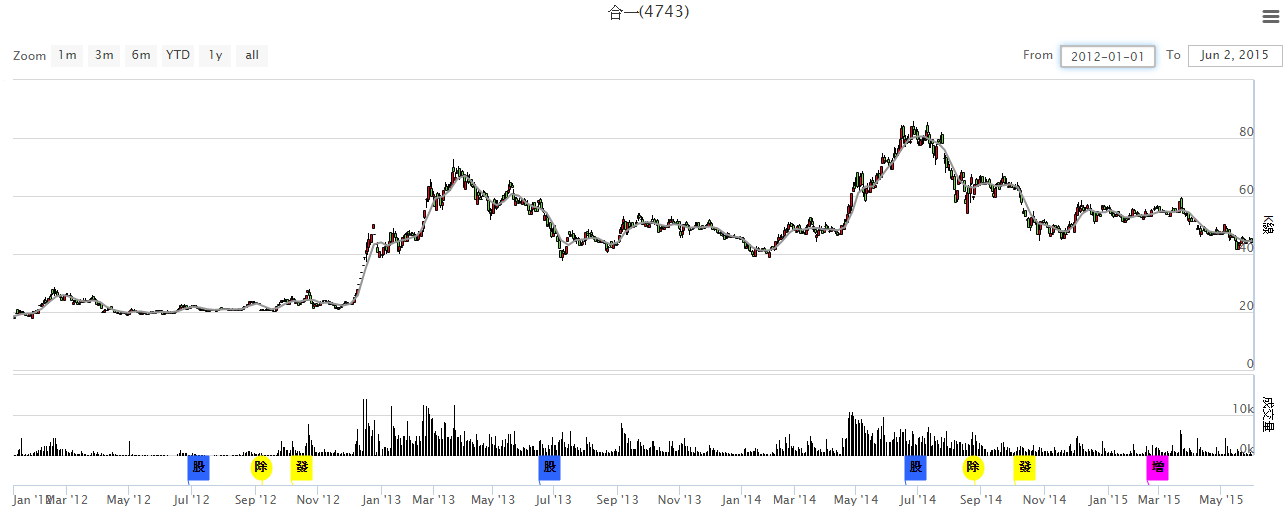
資料來源:股狗網
101/5/22
ON101 (WH-1)糖尿病傷口癒合新藥第二期人體臨床試驗通過GCP查核。
101/8/20
針對「用於治療糖尿病及新陳代謝疾病的組合物及其製備方法」,與高雄醫學大學簽訂技術移轉暨專利授權合約。本契約為全世界專屬授權,自簽約日起二十年有效。
101/12/25
基亞(3176-TW)股票及合一(4743-TW)因為漲幅過大,櫃買中心公告自25日起預收全部款券並每30分鐘撮合一次,因被處置,兩檔個股今天紛紛跌停開出並鎖住,處置期間則到年1月9日為止。
102/1/25
研發中糖尿病潰瘍傷口新藥ON101(WH-1) 第三期臨床試驗,今日獲代理人通知美國FDA同意於亞洲地區執行試驗。
102/2/19
「0B318」牛樟芝抗癌新藥及「0B412」糖尿病代謝 症候群新藥符合「生技新藥產業發展條例」,得適用該條例之投資獎勵。
102/5/22
牛樟芝(液態發酵菌絲體)產品完成91天毒理試驗證實具安全性。
102/8/5
與大陸石藥集團有限公司簽訂新藥與產品合作意向書。合作新藥項目包括OB318(牛樟芝抗肝癌)、左手香系列產品OB101(WH-1)將俟第三期臨床期中檢討後另行協商。
102/11/22
「極品牛樟芝菌絲體膠囊」通過 【保肝功效健康食品】查驗登記。
102/11/26
抗癌新藥OB318通過中華民國發明專利。
102/12/25
終止「用於治療糖尿病及新陳代謝疾病的組合物及其製備方法」技術移轉暨專利授權合約。經試驗後顯示產品有藥物動力學及安全性考量,雙方同意終止合約。
103/5/7
ON101糖尿病潰瘍傷口癒合新藥,衛生福利部核准執行多國多中心人體臨床試驗。
103/12/3
研發中新藥ON101(WH-1)糖尿病潰瘍傷口癒合新藥, 今日接獲香港衛生署(DOH)通知,准予執行第三期人體臨床試驗。
103/12/25
研發中新藥OB318牛樟芝抗肝癌新藥,今日通過 美國食品藥物管理局臨床試驗申請,准予執行第一期人體臨床試驗。
104/1/22
研發中新藥ON101(WH-1)糖尿病潰瘍傷口癒合新藥 ,今日接獲衛生福利部食品藥物管理署(TFDA)通知,准予執行人體藥物動力學臨床試驗。
104/5/4
研發中新藥OB318牛樟芝抗肝癌新藥,今日接獲 衛生福利部食品藥物管理署(TFDA)通知,准予執行第一期人體臨床試驗。
104/5/20
抗肝癌新藥OB318通過日本發明專利。
參考資料:
- 合一年報
- 公開資訊觀測站
- 聯合知識庫
- 植物新藥 http://goo.gl/tS1NrF
§本網站個股介紹僅就公司在產業趨勢中的機會、年報及新聞的整理,真正的公司評價仍需從總體經濟、財務資訊或公司經營等全方面著手,本整理所提供的資訊僅供參考,也無任何推介買賣之意,所有資訊仍應以資料來源公告為準。


