在台灣定義的藥物開發市場中,除了萬眾矚目的新成分開發,其實還有其他類別的研發也算是新藥−具備新療效複方或是新使用途徑的藥品,以及性質與新藥相近而被列入新藥:新劑型、新使用劑量、新單位含量之製劑。
根據藥事法施行細則:
新療效複方是指已核准藥品具有新適應症、降低副作用、改善療效強度、改善療效時間或改變使用劑量之新醫療效能,或二種以上已核准成分之複方製劑具有優於各該單一成分藥品之醫療效能者。
新使用途徑:指已核准藥品改變其使用途徑者。也就是說,如果市場上原有的藥品經過改良,大大降低副作用,則此新產品就算新藥;又如果原本只有口服劑型,而廠商開發出可以達到同樣或更好療效的貼片劑型,那麼即使是成分相同,這個貼片劑型仍然算是新藥。這樣的新藥研發聽起來是不是比完全「無中生有」來得簡單一點呢?
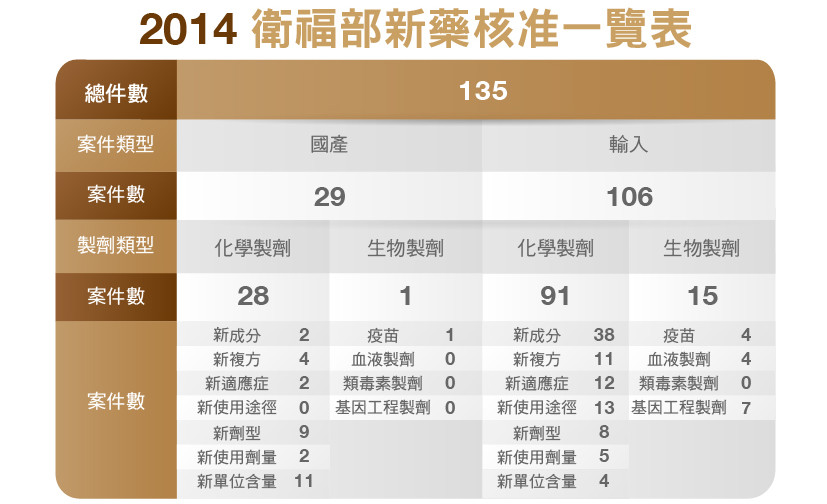
新成分新藥開發是一條漫長的路,不僅耗時花錢,更有可能竹籃子打水一場空,投入的風險極大,相較之下,以已上市的藥品為基礎去改良,藥品安全性已經過驗證,臨床試驗所花費的時間及成本皆較小,成功上市的機會較大。2014年衛福部統計資料顯示,所送審的國產新藥案件,28件中有26件為此類新藥,以中小規模為主的台灣廠商,的確看見自身的機會所在。
藥物傳輸系統(Drug Delivery Systems, DSS)-你要怎麼從台北到高雄?
從台北出發,可以選擇搭客運、台鐵、高鐵或是飛機,當然也可以選擇自行開車,且中途還可以繞道別的縣市,有無數條路徑可以抵達高雄。如同治療疾病時藥品的選擇,不論是口服、注射、貼片、塞劑等等不同的劑型,都是為了能讓藥品可以在病灶處作用。當然,劑型(交通工具)不同,吸收的快慢和程度(抵達與停留的時間)都會受到影響。
藥品的特性、劑型會影響其在人體內的吸收、分布、代謝及排除,導致服藥的頻率不同,有些一天需要服用3-4次,有些卻可以一天一次甚至一周一次,這也是為什麼同一個有效成分會出現口服、注射劑、貼片等等的不同劑型。藥品再有效,患者們因為不方便或是副作用過大而沒有按時服用也會讓效果大打折扣,所以在藥品開發過程中,除了安全性、有效性,方便性也是不容忽視的。
傳統藥劑學中所稱的『劑型』,已不足以描述其發展的程度與牽涉的層面,而今將研究如何將藥品送到病灶處,稱為藥物傳遞系統(Drug Delivery Systems, DDS)。透過調整劑型、技術等方法,利用不同配方組合或傳輸途徑,改變藥物的釋放吸收分佈,以達到提高療效、安全性、病患使用便利性及增強醫囑性等效果。藥物傳遞系統的應用範圍很廣泛,在口服、外用及注射劑型等等各類藥品上都可以使用。例如透過控制藥物的釋放避免在體內過早降解並提高吸收率;也可調控藥物釋放速率,以維持穩定的血中濃度;若提高藥物的靶向性,僅作用在患部則可降低副作用。
台灣廠商默默在這領域耕耘,已小有成果,也建立與國際大廠結盟的管道,如:
- 台微體(4152-TW)的微脂體傳輸技術,不但因技術轉移獲利之外,也有相關產品上市,在此領域可謂箇中翹楚;
- 健亞(4130-TW)的癌症化療止吐貼片,在臨床試驗第一期結果表現優良,即使競爭對手搶先一步上市,健亞也快速切換策略,轉以原廠授權學名藥身份快速切入市場;
- 泰合生技公司將自身定位於特色藥廠,發展Transdermal DDS經皮傳遞系統提升皮膚穿透力,適用劑型包括:貼片、膠體或是乳膏/霜等,與Transmucosal DDS傳遞技術所開發的口溶膜(Orally Dissolving Film, ODF),可分解並溶於口腔中之新劑型,能提供更便利給藥方式;
- 醫材廠匯特於2014年底宣布所開發的「多功能磁性奈米藥物載體」,獲台灣智慧財產局核發專利,具標靶新藥功能,整合了4大核心技術,包含藥物緩釋、磁性導引、核磁共振顯影特性及標靶定位。
還有很多廠商研發的專利技術族繁不及備載,可以確定的是台灣廠商已逐漸擺脫以往只能在學名藥市場競爭的劣勢。
藥物載體(Drug Carrier)−你要選擇什麼樣的交通工具?
1990年美國食品藥物管理局(Food and Drug Agency, FDA)核准了第一個使用藥物傳遞系統的抗細菌感染藥物Liposomal amphotericin B後,廠商更是積極投入藥物傳遞系統的研究,隨著技術不斷成熟輔以高科技的革新,其中較受矚目的藥物載體(Drug Carrier)傳輸技術,與奈米科技連動發展,各種創新的可降解性及生物相容性奈米載體,以及靶向性分子不斷被研發出來,此類的創新藥物載體技術主要被應用在治療癌症及感染性疾病的藥物上。
什麼是藥物載體呢?簡而言之就是裝載運輸藥品的物質,目的是用來提高藥物的療效、降低和減少藥物的毒副作用、減少給藥次數等等。所應用的載體材料,目前多為微脂體(Liposome)或高分子材料,如PLGA(poly(lactic-co-glycolic acid))、PCL(polycaprolactone),這兩類材料易攜帶藥品,具有高生物相容性及降解性。另外因其親/疏水性質的差異可用來攜帶不同的藥物。除了這兩類,其他無機材料奈米粒子也正被研究發展中,如前面所提的匯特藥廠的「多功能磁性奈米藥物載體」,所使用的就是奈米氧化鐵。
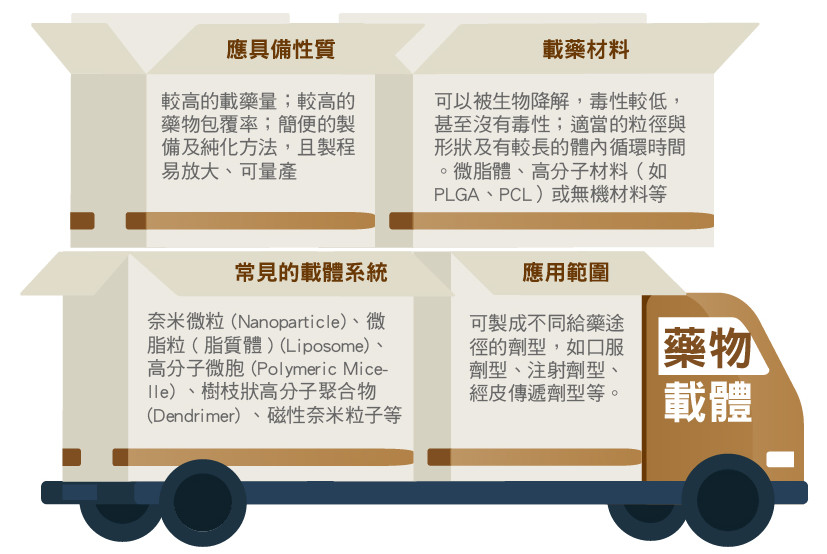
常見的藥物載體系統
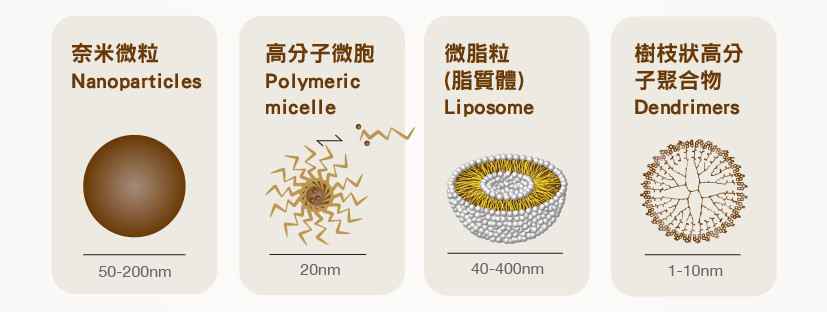
微脂體(脂質體Liposome)
談到經典藥物傳遞系統(DSS)發展例子,不能略過的就是微脂體。約莫在1965年,由英國劍橋Alec Bangham首度提出微脂體的概念,1971年英國萊門(Rymen)等人開始將脂質體用藥物載體。微脂體是由脂質雙層膜(lipid bilayer)所組成的微小球體,球粒直徑由幾十個毫微米(nm)到幾十個微米(μm)。能將藥物包覆於脂質微球,通過滲透或被巨噬細胞吞噬,微脂體載體被分解釋出藥物,從而產生作用。微脂體的脂質膜主要由磷脂質所構成,磷脂質的磷酸端為親水性,脂質端為疏水性,所以可以同時作為厭水性(Hydrophobic)及親水性(Hydrophilic)藥品的載體。
微脂體運用於藥物載體的特色
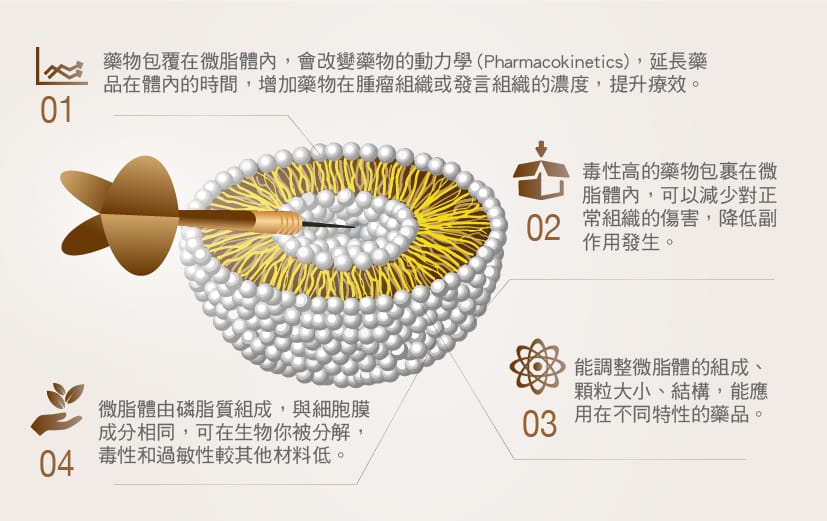
近幾年大分子藥物成為藥廠的新寵兒,不僅高技術門檻、高價值,且獲利高,研發的數量逐年攀升,然而即便如此,由於此類的藥品昂貴,並不是所有患者都有能力負擔,目前臨床上的抗癌藥物大多還是使用高生物毒性的小分子藥物,傳統的抗癌藥品選擇性低,容易影響或累積於身體其他正常器官或組織,造成嚴重副作用。而微脂體的問世及技術越趨成熟的助益下,帶來一線曙光。
Doxorubicin(俗稱小紅莓),是一廣泛使用於多種癌症的傳統抗癌藥物,然而因為除了殺死癌細胞之外,也會影響正常組織與器官,除了一般常見的化療副作用,如噁心嘔吐、黏膜組織發炎和落髮之外,對心臟會產生累積性的毒性,甚至有致命風險。現利用平均直徑約100nm的微脂體包覆Doxorubicin,因其粒徑性質可避免藥物滲入正常組織中,而腫瘤組織可能發生血管壁縫隙擴大,讓藥物可以腫瘤組織累積達到治療效果。這種針對特定組織或器官的選擇性輸送特性稱為靶向性(Targeting)。
當然微脂體的應用不止於此,還包括疫苗的發展、基因治療、免疫調控藥劑等等。台灣微脂體技術領導廠商更利用所長與國際藥廠結盟,將微脂體包裹技術與標靶抗體結合,應用在癌症治療。目前熱門的技術之一,是結合抗體與小分子藥物的技術ADC(Antibody Drug Conjugate),因為可以利用抗體的標靶性藥效強但的性高的小分子藥物精準傳遞至病灶處,以降低副作用的產生;而標靶微脂體技術更可以提高攜藥量,大幅提高療效。
洞燭機先,展望未來
其實美國FDA核准的新藥中,也有大半的比例是新劑型及新藥物傳輸途徑。因為新劑型新藥的主成份已經過驗證,安全性疑慮較低,可將研發時間縮短至5-7年,且成功率提高。更重要的是這個市場不像學名藥,競爭激烈,這也是讓擁有關鍵技術的廠商能夠吸引國際大廠的青睞。
台灣生技產業在政府培植與廠商不斷投入下,研發產能已有一定基礎,加上台灣領導廠商相繼與國際大廠合作結盟,推展了台灣生技業在國際的知名度,新劑型新藥可謂另一個極具發展潛力的市場,而在能不能這片天空翱翔的關鍵是掌握專利技術。



訂閱制後的營收變化_.png)